và gửi cho chúng tôi
Chiều 31/5, Bộ trưởng Bộ Y tế Nguyễn Thanh Long cho biết, thực hiện Kết luận của Bộ Chính trị cũng như Nghị quyết 21 của Chính phủ, trong thời gian qua, Bộ Y tế đã phối hợp với tất cả các bộ, ban ngành cũng như khuyến khích tất cả các địa phương, doanh nghiệp, đơn vị tham gia vào tìm kiếm, nhập khẩu vaccine phòng COVID-19 để có nguồn vaccine sử dụng cho người dân Việt Nam nhanh nhất, sớm nhất và rộng nhất.
Tới đây, Bộ Y tế tiếp tục đưa ra các chính sách khuyến khích, động viên nhiều hơn các địa phương, doanh nghiệp tham gia vào quá trình tìm kiếm vaccine phòng COVID-19.
CĂN CỨ PHÁP LÝ:
-Luật Dược số 105/2016/QH13 ngày 06/04/2016
-Nghị định số
54/2017/NĐ-CP ngày 08/05/2017 của Chính phú quy định
chi tiết một số điều và biện pháp thi hành Luật
dược
-Nghị định số
155/2018/NĐ-CP ngày 12/11/2018 của Chính phủ sửa đổi,
bổ sung một số quy định liên quan đến điều kiện
đầu tư kinh doanh thuộc phạm
vi quản lý nhà nước của Bộ Y tế
Bộ Y tế sẽ tạo điều kiện tối đa cho tất cả các địa phương và đơn vị, doanh nghiệp trong quá trình nhập khẩu, cấp phép nhập khẩu, kiểm định vaccine. Thủ tục nhập khẩu Vắc Xin phụ thuộc vào loại vắc xin mà doanh nghiệp nhập khẩu
I.Đối với vắc xin đã được Tổ chức Y tế thế giới (WHO) phê duyệt
Với các vắc xin đã được Tổ chức Y tế
thế giới (WHO) phê duyệt sử dụng trong tình trạng
khẩn cấp (từ các cơ sở sản xuất: AstraZeneca, Pfizer, Moderna,
Sinopharm, Johnson & Johnson …), Bộ Y tế sẽ
xem xét phê duyệt trong thời gian 05 ngày làm việc
khi nhận đủ hồ sơ hợp pháp, hợp lệ và kèm theo ủy quyền chính thức của cơ sở sản xuất vắc xin phòng Covid-19.
II. Đối với vắc xin chưa được Tổ chức Y tế
thế giới (WHO) phê duyệt
- Với các vắc xin đã được các quốc gia khác phê
duyệt nhưng chưa được WHO
phê duyệt sử dụng trong tình trạng khẩn cấp, Bộ
Y tế sẽ xem xét, phê duyệt trong thời gian 10 ngày
làm việc khi nhận được đủ hồ sơ hợp pháp, hợp lệ và kèm theo ủy quyền chính thức của cơ sở sản xuất vắc xin phòng Covid-19.
- Khi làm thủ tục nhập khẩu vắc xin vào Việt
Nam, các đơn vị gửi hồ sơ chất lượng theo quy định
(bao gồm: Giấy chứng nhận xuất xưởng của cơ sở sản xuất
và/hoặc Giấy chứng nhận chất lượng của cơ quan quản lý) để Viện Kiểm định Quốc gia vắc xin và sinh phẩm y tế (NICVB) thực hiện việc
cấp Giấy chứng nhận xuất xưởng trong vòng 48 giờ
theo khuyến cáo của WHO để đảm bảo chất lượng,
tránh việc nhập khẩu vắc xin không rõ nguồn gốc.
III. Vắc xin được Bộ Y Tế Việt Nam phê duyệt có điều kiện cho nhu cầu cấp bách trong phòng, chống dịch bệnh covid-19
A. COVID-19 Vaccine AstraZeneca
1. Tên vắc xin: COVID-19 Vaccine AstraZeneca
2. Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều (0,5ml) chứa: vắc xin COVID-19 (ChAdOx1-S tái tổ hợp) 5 x 1010 hạt vi rút (vp).
3 Dạng bào chế: Dung dịch tiêm.
4. Quy cách đóng gói:
a) Hộp 10 lọ, mỗi lọ chứa 8 liều, mỗi liều 0,5ml;
b) Hộp 10 lọ, mỗi lọ chứa 10 liều, mỗi liều 0,5ml.
5. Tên cơ sở sản xuất - Nước sản xuất:
a) Catalent Anagni S.R.L - Ý.
b) CP Pharmaceuticals Limited - Anh.
c) IDT Biologika GmbH - Đức.
B. Gam-COVID-Vac
1. Tên vắc xin: Gam-COVID-Vac (tên khác là SPUTNIK V).
2. Thành phần hoạt chất, nồng độ/hàm lượng:
- Mỗi liều 0,5ml thành phần I (mũi tiêm 1): Chứa (1,0 ± 0,5) x 1011 hạt vi rút Adeno typ huyết thanh 26 của người tái tổ hợp mang gen mã hóa protein S của SARS-CoV-2.
- Mỗi liều 0,5ml thành phần II (mũi tiêm 2): Chứa (1,0 ± 0,5) x 1011 hạt vi rút Adeno typ huyết thanh 5 của người tái tổ hợp mang gen mã hóa protein S của SARS-CoV-2
3. Dạng bào chế: Dung dịch tiêm.
4. Quy cách đóng gói: Hộp 1 lọ 3ml (chứa 5 liều).
5. Tên cơ sở sản xuất - Nước sản xuất: JSC Generium - Liên Bang Nga.
6. Tên cơ sở đề nghị phê duyệt vắc xin: Trung tâm nghiên cứu, sản xuất vắc xin và Sinh phẩm y tế (POLYVAC).
C. COVID-19 Vaccine (Vero Cell), Inactivated
1. Tên vắc xin: COVID-19 Vaccine (Vero Cell), Inactivated (tên khác là SARS-CoV-2 Vaccine (Vero Cell), Inactivate).
2. Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều 0,5ml chứa 6.5U kháng nguyên SARS-CoV-2 bất hoạt.
3. Dạng bào chế: Hỗn dịch tiêm.
4. Quy cách đóng gói:
- Hộp 1 lọ, 3 lọ; mỗi lọ chứa 1 liều 0,5ml.
- Hộp 1 bơm tiêm chứa 1 liều 0,5ml.
5. Tên cơ sở sản xuất - Nước sản xuất: Beijing Institute of Biological Products Co., Ltd. - Trung Quốc.
6. Tên cơ sở đề nghị phê duyệt vắc xin: Viện Vệ sinh dịch tễ Trung ương.
Bạn đọc đừng quên theo
dõi Khánh An mỗi ngày để nâng cao kiến thức pháp lý và chủ động bảo vệ tốt nhất
quyền lợi của mình. Nếu có bất cứ vướng mắc nào hoặc có nhu cầu thành lập công
ty, đừng ngại liên hệ với Khánh An để được tư vấn trực tiếp. CÔNG TY LUẬT TNHH KHÁNH AN BUSINESS LAW Văn phòng: Toà nhà 88 Tô Vĩnh Diện, Khương Đình, Hà Nội Hotline: 097.652.9499
hoặc 097.652.9499 Email:
info@khanhanlaw.net Website:https://khanhanlaw.com/
Khuyến cáo:
Bài viết này chỉ nhằm mục đích cung cấp các thông tin chung và không nhằm cung cấp bất kỳ ý kiến tư vấn cho bất kỳ trường hợp cụ thể nào. Các quy định pháp luật được dẫn chiếu trong nội dung bài viết có hiệu lực vào thời điểm đăng tải bài viết nhưng có thể đã hết hiệu lực tại thời điểm bạn đọc. Do đó, chúng tôi khuyến nghị bạn luôn tham khảo ý kiến của chuyên gia trước khi áp dụng.
Các vấn đề liên quan đến nội dung hoặc quyền sở hữu trí tuệ của bài viết, vui lòng gửi email đến info@khanhanlaw.net.
Khánh An là một công ty tư vấn tại Việt Nam có kinh nghiệm và năng lực cung cấp các dịch vụ tư vấn liên quan đến Doanh nghiệp và Đầu tư. Vui lòng tham khảo về dịch vụ của chúng tôi qua website: khanhanlaw.com hoặc liên hệ trực tiếp qua số Hotline: 097.652.9499.
 Trước năm 2022, trang thiết bị y tế nhóm C,D không bắt buộc phải đăng ký lưu hành mà có thể xin giấy phép nhập khẩu hoặc công khai phân loại đối với trang thiết bị y tế không thuộc danh mục phải phê duyệt cấp phép nhập khẩu. Từ 01/01/2022 nghị định 98/2021/NĐ-CP có hiệu lực, đăng ký lưu hành trang thiết bị y tế nhóm C,D phải đăng ký lưu hành. Tuy tại điều khoản chuyển tiếp một số trang thiết bị y tế được phép tiếp tục nhập khẩu đến 31/12/2022, nhưng do tính chất đặc thù của trang thiết bị y tế, một số cơ quan hải quan vẫn yêu cầu buộc phải có số lưu hành trang thiết bị y tế để thông quan hàng hóa. Cùng Khánh An tìm hiểu dịch vụ đăng ký lưu hành trang thiết bị y tế nhóm C,D trong bài viết sau:
Trước năm 2022, trang thiết bị y tế nhóm C,D không bắt buộc phải đăng ký lưu hành mà có thể xin giấy phép nhập khẩu hoặc công khai phân loại đối với trang thiết bị y tế không thuộc danh mục phải phê duyệt cấp phép nhập khẩu. Từ 01/01/2022 nghị định 98/2021/NĐ-CP có hiệu lực, đăng ký lưu hành trang thiết bị y tế nhóm C,D phải đăng ký lưu hành. Tuy tại điều khoản chuyển tiếp một số trang thiết bị y tế được phép tiếp tục nhập khẩu đến 31/12/2022, nhưng do tính chất đặc thù của trang thiết bị y tế, một số cơ quan hải quan vẫn yêu cầu buộc phải có số lưu hành trang thiết bị y tế để thông quan hàng hóa. Cùng Khánh An tìm hiểu dịch vụ đăng ký lưu hành trang thiết bị y tế nhóm C,D trong bài viết sau:
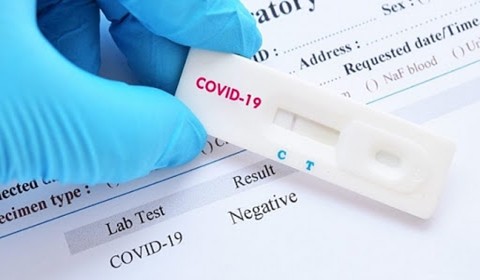 Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus và xét nghiệm tìm kháng thể do cơ thể sinh ra để chống lại virut. Test nhanh covid 19 phát hiện kháng nguyên covid 19 hiện nay đang được ứng dụng rộng rãi để sàng lọc diện rộng nhằm phát hiện covid 19.
Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus và xét nghiệm tìm kháng thể do cơ thể sinh ra để chống lại virut. Test nhanh covid 19 phát hiện kháng nguyên covid 19 hiện nay đang được ứng dụng rộng rãi để sàng lọc diện rộng nhằm phát hiện covid 19.
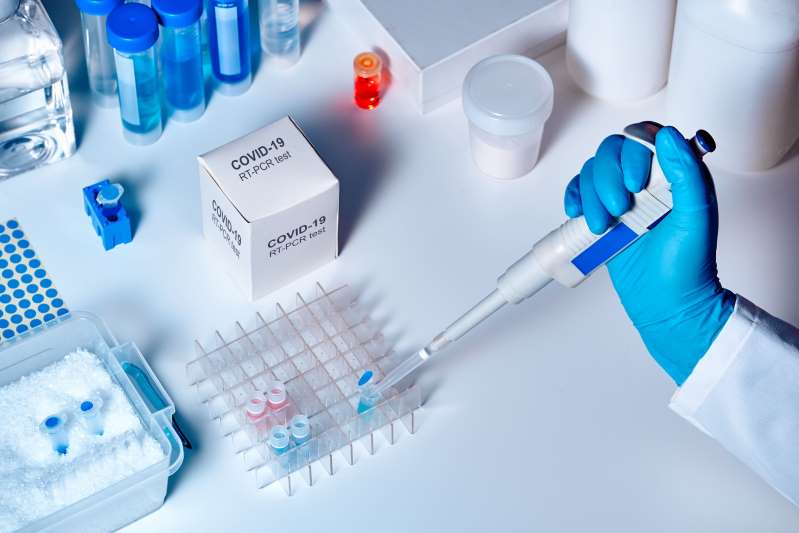 Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus. Test phát hiện kháng nguyên virus SarS-CoV-2 là gì? Kit xét nghiệm đa chỉ tiêu SARS-CoV-2 RT-PCR là hóa chất chuẩn đoán dùng trong xét nghiệm định tính RNA từ vi-rút SARS-CoV-2 bằng phương pháp Real-Time RT-PCR từ các mẫu bệnh phẩm đường hô hấp trên như mẫu phết dịch mũi họng và mẫu phết dịch hầu họng.
Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus. Test phát hiện kháng nguyên virus SarS-CoV-2 là gì? Kit xét nghiệm đa chỉ tiêu SARS-CoV-2 RT-PCR là hóa chất chuẩn đoán dùng trong xét nghiệm định tính RNA từ vi-rút SARS-CoV-2 bằng phương pháp Real-Time RT-PCR từ các mẫu bệnh phẩm đường hô hấp trên như mẫu phết dịch mũi họng và mẫu phết dịch hầu họng.