và gửi cho chúng tôi
Việc đánh giá đáp ứng Thực hành tốt của cơ sở thử nghiệm không vì mục đích thương mại thực hiện theo quy định về Thực hành tốt do Bộ trưởng Bộ Y tế ban hành. Vậy thủ tục xin giấy chứng nhận Thực hành tốt phòng thí nghiệm đối với cơ sở thử nghiệm không vì mục đích thương mại có dễ thực hiện không, hồ sơ cần phải chuẩn bị những gì? Hãy cùng Khánh An tìm hiểu sau đây.
- Luật dược số 105/2016/QH13 ngày 06 tháng 4 năm 2016.
- Nghị định số 54/2017/NĐ-CP ngày 8/5/2017 của
Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật dược.
- Thông tư số 04/2018/TT-BYT ngày 09/02/2018
của Bộ Y tế quy định về Thực hành tốt phòng thí nghiệm
-Thông tư số 277/2016/TT-BYT ngày 14/11/2016
của Bộ Tài chính quy định mức thu, chế độ thu, nộp, quản lý và sử dụng phí
trong lĩnh vực dược, mỹ phẩm.
Cơ sở quy định
tại Điểm a Khoản 1 Điều này phải tuân thủ điều kiện kinh doanh quy định tại Khoản
1 Điều 33 của Luật dược 2016;
Cơ sở thử
nghiệm phải có địa điểm, khu vực bảo quản, trang thiết bị bảo quản, tài liệu
chuyên môn kỹ thuật và nhân sự đáp ứng Thực hành tốt cơ sở thử nghiệm; đối với
cơ sở chuyên thử nghiệm dược liệu, thuốc dược liệu, thuốc cổ truyền thực hiện
theo quy định tại Điểm b Khoản 2 Điều 69 của Luật dược 2016.
§
Đơn đề nghị đánh giá đáp ứng GLP thực hiện
theo Mẫu số 01 quy định tại Phụ lục V kèm theo Thông tư 04/2018/TT-BYT;
§
Tài liệu kỹ thuật về cơ sở thử nghiệm được
trình bày theo hướng dẫn về hồ sơ tổng thể quy định tại Phụ lục III kèm theo
Thông tư 04/2018/TT-BYT.
Khanh An Consultant cung cấp dịch vụ xin Giấy
chứng nhận Thực hành tốt phòng thí nghiệm
Bước 1: Cơ sở thử nghiệm không vì mục
đích thương mại gửi hồ sơ về Cục Quản lý dược - Bộ Y tế
Bước 2: Sau khi nhận hồ sơ, Cục Quản lý dược trả cho cơ sở Phiếu tiếp
nhận hồ sơ. Cơ sở nộp hồ sơ sửa đổi, bổ sung (nếu có)
Bước 3: Trong thời hạn 05 ngày, kể từ ngày nhận được
hồ sơ hợp lệ, Cục Quản lý dược thành lập Đoàn đánh giá, thông báo
cho cơ sở thử nghiệm về Đoàn đánh giá và dự kiến thời gian đánh giá thực
tế tại cơ sở.
Bước 4: Trong thời hạn 10 ngày, kể từ ngày kết thúc
việc đánh giá thực tế tại cơ sở thử nghiệm và ký biên bản đánh giá, Cục Quản lý Dược cấp Giấy chứng nhận GLP
theo Mẫu số 04 quy định tại Phụ lục V kèm
theo Thông tư này cho cơ sở thử nghiệm không vì Mục đích thương mại
Bước
5: Trong thời hạn 05 ngày, kể từ ngày cấp Giấy chứng
nhận GLP, Cục Quản lý dược công bố Trên Trang thông tin điện tử của
Sở
|
TÊN
ĐƠN VỊ CHỦ QUẢN |
CỘNG
HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM |
|
Số: ………/…...
|
……….,
ngày ……. tháng ….. năm 20….
|
ĐƠN ĐĂNG KÝ KIỂM TRA
THỰC HÀNH TỐT PHÒNG THÍ NGHIỆM
(Đăng ký kiểm tra lần đầu)
Kính gửi: Cục Quản lý Dược - Bộ Y tế
Tên
cơ sở:
Địa
chỉ công
ty/cơ sở kiểm nghiệm:
Điện
thoại/fax/email:
Thực
hiện Thông tư số 04/2018/TT-BYT ngày 09/02/2018của Bộ Y tế quy định về Thực
hành tốt phòng thí nghiệm và hướng dẫn việc triển khai, áp dụng, sau khi tiến
hành tự thanh tra và đánh giá đạt yêu cầu; cơ sở chúng tôi xin đăng ký với
Bộ Y tế (Cục Quản lý Dược) kiểm tra GLP vào bất kỳ thời gian nào và cam kết
khắc phục kịp thời những tồn tại ghi trong biên bản kiểm tra.
Chúng
tôi xin gửi kèm bản đăng ký này các tài liệu liên quan sau đây:
(1)-
Tài liệu pháp lý chứng minh việc thành lập và chức năng nhiệm vụ
của đơn vị.
(2)-
Bản sao chứng
thực Chứng chỉ hành
nghề dược của người phụ trách chuyên môn về dược.
(3)- Bản
hồ sơ tổng thể về cơ sở kiểm nghiệm thuốc, nguyên liệu làm
thuốc.
|
|
Phụ
trách cơ sở kiểm nghiệm |
Ø
Tư vấn đến Quý khách hàng điều kiện
xin cấp Giấy chứng nhận
Thực hành tốt phòng thí nghiệm theo quy định mới nhất
Ø
Soạn thảo bộ hồ sơ xin dánh giá Thực hành tốt phòng thí nghiệm đối
với cơ sở kinh doanh đầy đủ, chính xác;
Ø
Thay mặt Quý khách hàng nộp hồ sơ và thực hiện các thủ tục tại cơ
quan nhà nước có thẩm quyền;
Ø
Theo dõi hồ sơ và bổ sung theo yêu cầu của cơ quan nhà nước (nếu
có);
Ø
Duy trì hệ thống hồ sơ tài liệu theo GLP cho các lần đánh giá tiếp
theo;
Ø
Tư vấn các vấn đề liên quan.
Xem thêm:
UY TÍN – CHẤT LƯỢNG – HIỆU QUẢ CAO là những giá trị chúng
tôi mang lại cho Quý khách hàng. Đáp lại những giá trị đó là những phản hồi rất
tích cực đã mang lại động lực cho Khánh An phát triển như ngày hôm nay. Mọi
thắc mắc vui lòng liên hệ ngay với chúng tôi!
Thông tin liên hệ:
Address: Toà nhà 88 Tô Vĩnh Diện, Khương Đình, Hà Nội
Mobile: 097.652.9499- 097.652.9499
Web: Khanhanlaw.com
Email: Info@khanhanlaw.net
Rất hân hạnh được hợp tác cùng Quý khách!
Khuyến cáo:
Bài viết này chỉ nhằm mục đích cung cấp các thông tin chung và không nhằm cung cấp bất kỳ ý kiến tư vấn cho bất kỳ trường hợp cụ thể nào. Các quy định pháp luật được dẫn chiếu trong nội dung bài viết có hiệu lực vào thời điểm đăng tải bài viết nhưng có thể đã hết hiệu lực tại thời điểm bạn đọc. Do đó, chúng tôi khuyến nghị bạn luôn tham khảo ý kiến của chuyên gia trước khi áp dụng.
Các vấn đề liên quan đến nội dung hoặc quyền sở hữu trí tuệ của bài viết, vui lòng gửi email đến info@khanhanlaw.net.
Khánh An là một công ty tư vấn tại Việt Nam có kinh nghiệm và năng lực cung cấp các dịch vụ tư vấn liên quan đến Doanh nghiệp và Đầu tư. Vui lòng tham khảo về dịch vụ của chúng tôi qua website: khanhanlaw.com hoặc liên hệ trực tiếp qua số Hotline: 097.652.9499.
 Trước năm 2022, trang thiết bị y tế nhóm C,D không bắt buộc phải đăng ký lưu hành mà có thể xin giấy phép nhập khẩu hoặc công khai phân loại đối với trang thiết bị y tế không thuộc danh mục phải phê duyệt cấp phép nhập khẩu. Từ 01/01/2022 nghị định 98/2021/NĐ-CP có hiệu lực, đăng ký lưu hành trang thiết bị y tế nhóm C,D phải đăng ký lưu hành. Tuy tại điều khoản chuyển tiếp một số trang thiết bị y tế được phép tiếp tục nhập khẩu đến 31/12/2022, nhưng do tính chất đặc thù của trang thiết bị y tế, một số cơ quan hải quan vẫn yêu cầu buộc phải có số lưu hành trang thiết bị y tế để thông quan hàng hóa. Cùng Khánh An tìm hiểu dịch vụ đăng ký lưu hành trang thiết bị y tế nhóm C,D trong bài viết sau:
Trước năm 2022, trang thiết bị y tế nhóm C,D không bắt buộc phải đăng ký lưu hành mà có thể xin giấy phép nhập khẩu hoặc công khai phân loại đối với trang thiết bị y tế không thuộc danh mục phải phê duyệt cấp phép nhập khẩu. Từ 01/01/2022 nghị định 98/2021/NĐ-CP có hiệu lực, đăng ký lưu hành trang thiết bị y tế nhóm C,D phải đăng ký lưu hành. Tuy tại điều khoản chuyển tiếp một số trang thiết bị y tế được phép tiếp tục nhập khẩu đến 31/12/2022, nhưng do tính chất đặc thù của trang thiết bị y tế, một số cơ quan hải quan vẫn yêu cầu buộc phải có số lưu hành trang thiết bị y tế để thông quan hàng hóa. Cùng Khánh An tìm hiểu dịch vụ đăng ký lưu hành trang thiết bị y tế nhóm C,D trong bài viết sau:
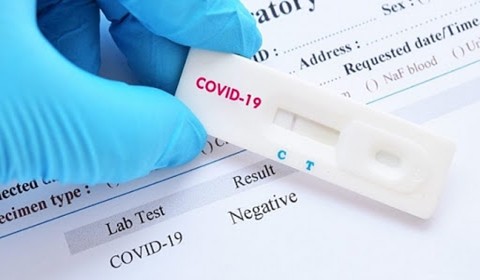 Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus và xét nghiệm tìm kháng thể do cơ thể sinh ra để chống lại virut. Test nhanh covid 19 phát hiện kháng nguyên covid 19 hiện nay đang được ứng dụng rộng rãi để sàng lọc diện rộng nhằm phát hiện covid 19.
Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus và xét nghiệm tìm kháng thể do cơ thể sinh ra để chống lại virut. Test nhanh covid 19 phát hiện kháng nguyên covid 19 hiện nay đang được ứng dụng rộng rãi để sàng lọc diện rộng nhằm phát hiện covid 19.
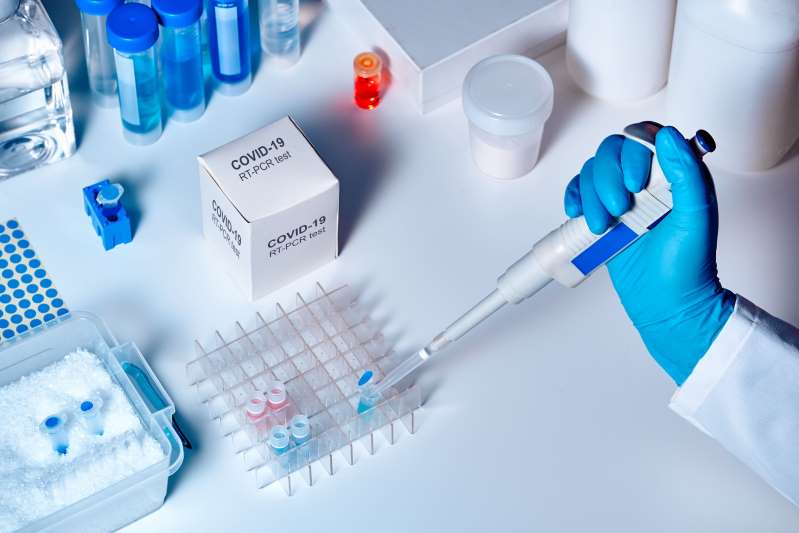 Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus. Test phát hiện kháng nguyên virus SarS-CoV-2 là gì? Kit xét nghiệm đa chỉ tiêu SARS-CoV-2 RT-PCR là hóa chất chuẩn đoán dùng trong xét nghiệm định tính RNA từ vi-rút SARS-CoV-2 bằng phương pháp Real-Time RT-PCR từ các mẫu bệnh phẩm đường hô hấp trên như mẫu phết dịch mũi họng và mẫu phết dịch hầu họng.
Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus. Test phát hiện kháng nguyên virus SarS-CoV-2 là gì? Kit xét nghiệm đa chỉ tiêu SARS-CoV-2 RT-PCR là hóa chất chuẩn đoán dùng trong xét nghiệm định tính RNA từ vi-rút SARS-CoV-2 bằng phương pháp Real-Time RT-PCR từ các mẫu bệnh phẩm đường hô hấp trên như mẫu phết dịch mũi họng và mẫu phết dịch hầu họng.