và gửi cho chúng tôi
Kỹ thuật xét nghiệm Real-Time PCR (Polymerase Chain Reaction) đang ngày càng trở nên phổ biến nhờ kỹ thuật khuếch đại định danh và mô tả chính xác những tác nhân gây bệnh, hỗ trợ hiệu quả trong việc chuẩn đoán bệnh.
1.
PCR là gì?
Cụm từ PCR được viết tắt từ Polymerase Chain Reaction mang
nghĩa là chuỗi phản ứng polymerase hay phản ứng khuếch đại gen. PCR là một kỹ thuật được sử dụng để khuếch đại một
đoạn DNA hoặc sản xuất và nhân bản nhiều mẫu DNA giống nhau theo cấp lũy thừa,
tạo ra hàng ngàn đến hàng triệu bản sao của một trình tự DNA nào đó từ một mẫu
nhỏ ban đầu hoặc là một bản sao duy nhất.
DNA là phân tử mang thông tin di truyền dưới dạng bộ ba mã di
truyền quy định mọi hoạt động sống (sinh trưởng, sinh sản, phát triển v.v) của
các sinh vật và hầu hết virus. Đây là từ viết tắt thuật ngữ tiếng Anh
deoxyribonucleic acid.
Kỹ thuật xét nghiệm Real-Time PCR (Polymerase Chain Reaction)
được sử dụng nhằm khuếch đại và cùng lúc xác định được số lượng của phân tử DNA
đích. Xét nghiệm Realtime PCR trở nên hữu dụng để định danh và mô tả chính xác
những tác nhân gây bệnh
(Máy PCR )
2.
Phân loại rủi ro
Dự kiến phân loại rủi ro D theo thông tư 39/2016/TT-BYT
3. Thủ tục nhập khẩu:
3.1 Căn cứ pháp lý:
- Nghị
định 36/2016/NĐ-CP về quản lý trang thiết bị y tế
- Thông
tư 13/2021/TT-BYT về quy định cấp số lưu hành, nhập khẩu trang thiết bị y tế phục
vụ phòng, chống dịch COVID-19 trong trường hợp cấp bách;
- Thông tư 39/2016/TT-BYT về phân loại trang thiết bị y tế
3.2 Thủ tục nhập khẩu:
1. Cơ sở đề nghị cấp giấy chứng nhận đăng ký lưu hành nộp trực
tiếp hồ sơ theo quy định tại Điều 8 Thông tư này tại Vụ Trang thiết bị và Công
trình y tế. Đối với các hồ sơ nộp qua đường bưu điện thực hiện theo quy định tại
Quyết định số 45/2016/QĐ-TTg ngày 19 tháng 10 năm 2016 của Thủ tướng Chính phủ
về việc tiếp nhận hồ sơ, trả kết quả giải quyết thủ tục hành chính qua dịch vụ
bưu chính công ích.
2. Sau khi nhận được hồ sơ đầy đủ, hợp lệ (bao gồm cả giấy tờ
xác nhận đã nộp phí thẩm định cấp giấy phép lưu hành theo quy định của Bộ Tài
chính), Vụ Trang thiết bị và Công trình y tế thực hiện:
a) Đóng dấu tiếp nhận hồ sơ trên cả hai văn bản đề nghị cấp
giấy chứng nhận đăng ký lưu hành và trả lại cho cơ sở đề nghị 01 bản (D ấu tiếp
nhận phải thể hiện đầy đủ giờ, ngày tháng năm tiếp nhận hồ sơ);
b) Thực hiện quy trình thẩm định, cấp giấy ch ứng nhận đăng
ký lưu hành theo quy định tại khoản 3 Điều này.
3. Thẩm định,
cấp giấy chứng nhận đăng ký lưu hành:
a) Trường hợp không có yêu cầu sửa đổi, bổ sung hồ sơ: Vụ
Trang thiết bị và Công trình y tế tổ chức thẩm định các giấy tờ quy định tại
các khoản 1, 3, 4, 5, 6 Điều 8 Thông tư này và điểm d khoản 1 Điều 26 Nghị định
số 36/2016/NĐ-CP để cấp mới giấy chứng nhận đăng ký lưu hành trong thời hạn 10
ngày làm việc, kể từ ngày tiếp nhận hồ sơ (ngày tiếp nhận hồ sơ được tính theo
ngày ghi trên dấu công văn đến của Vụ Trang thiết bị và Công trình y tế). Trường
hợp không cấp giấy chứng nhận đăng ký lưu hành phải có văn bản trả lời và nêu
rõ lý do;
Trong thời hạn tối đa 03 ngày làm việc, kể từ ngày cấp giấy
chứng nhận đăng ký lưu hành, Vụ Trang thiết bị và Công trình y tế có trách nhiệm
công khai toàn bộ hồ sơ đăng ký lưu hành trên cổng thông tin điện tử Hệ thống dịch
vụ công trực tuyến quản lý trang thiết bị y tế, tại địa chỉ:
https://dmec.moh.gov.vn.
b) Trường hợp hồ sơ đề nghị cấp giấy chứng nhận đăng ký lưu
hành chưa hoàn chỉnh:
- Vụ Trang thiết bị và Công trình y tế phải có văn bản thông
báo cho tổ chức đề nghị cấp số lưu hành để bổ sung, sửa đổi hồ sơ trong thời hạn
03 ngày làm việc, kể từ ngày nhận được hồ sơ đề nghị cấp giấy ch ứng nhận đăng
ký lưu hành, trong đó phải nêu cụ thể là bổ sung những tài liệu nào, nội dung
nào cần sửa đổi;
- Khi nhận được văn bản yêu cầu bổ sung, sửa đổi hồ sơ đề nghị
cấp giấy chứng nhận đăng ký lưu hành, cơ sở đề nghị cấp giấy chứng nhận đăng ký
lưu hành phải bổ sung, sửa đổi theo đúng những nội dung đã được ghi trong văn bản
và gửi về Bộ Y tế.
c) Trường hợp cơ sở đề nghị cấp giấy chứng nhận đăng ký lưu
hành đã bổ sung, sửa đổi hồ sơ nhưng không đúng với yêu cầu thì Bộ Y tế sẽ
thông báo cho cơ sở để tiếp tục hoàn chỉnh hồ sơ theo quy định tại điểm b khoản
3 Điều này;
d) Sau 30 ngày, kể từ ngày Vụ Trang thiết bị và Công trình y
tế có văn bản yêu cầu mà cơ sở không bổ sung, sửa đổi hồ sơ hoặc nếu sau 03 lần
sửa đổi, bổ sung hồ sơ kể từ ngày Vụ Trang thiết bị và Công trình y tế có yêu cầu
sửa đổi, bổ sung lần đầu mà hồ sơ vẫn không đáp ứng yêu cầu thì phải thực hiện
lại từ đầu thủ tục đề nghị cấp giấy chứng nhận đăng ký lưu hành.
Xem thêm:...
Thủ tục nhập khẩu máy đo nồng đô oxi trong máu...
Dịch vụ xin Giấy phép nhập khẩu Test Covid sử dụng với máy PCR
----------------
Là một trong những đơn
vị dẫn đầu trong lĩnh vực tư vấn xin giấy phép về trang thiết bị y tế, Khánh An
sẽ giúp Quý khách hoàn tất hồ sơ một cách nhanh chóng nhất. Việc xin Giấy phép
trang thiết bị y tế sẽ nhanh chóng và dễ dàng hơn bao giờ hết. Với đội ngũ nhân
viên am hiểu luật, trình tự hồ sơ, chúng tôi sẽ luôn giúp Quý khách tìm được giải
pháp hiệu quả, tiết kiệm chi phí nhất.
Quý khách hàng có thắc
mắc hoặc có nhu cầu sử dụng dịch vụ xin Giấy phép trang thiết bị y tế, hãy liên
hệ ngay cho chúng tôi qua số hotline: 02466 885 821 hoặc 096 987 7894 để được
NHẬN TƯ VẤN MIỄN PHÍ. Quý khách cũng có thể truy cập vào website của chúng tôi:
https://khanhanlaw.com/ để tham khảo các thông tin về tư vấn luật chính xác và
nhận tư vấn miễn phí qua điện thoại!
Thông tin liên hệ:
CÔNG TY LUẬT TNHH KHÁNH AN BUSINESS LAW
Địa chỉ: Toà nhà 88 Tô Vĩnh Diện, Khương Trung, Thanh Xuân,
Hà Nội.
Hotline: 097.652.9499.
Email: info@khanhanlaw.net
Khuyến cáo:
Bài viết này chỉ nhằm mục đích cung cấp các thông tin chung và không nhằm cung cấp bất kỳ ý kiến tư vấn cho bất kỳ trường hợp cụ thể nào. Các quy định pháp luật được dẫn chiếu trong nội dung bài viết có hiệu lực vào thời điểm đăng tải bài viết nhưng có thể đã hết hiệu lực tại thời điểm bạn đọc. Do đó, chúng tôi khuyến nghị bạn luôn tham khảo ý kiến của chuyên gia trước khi áp dụng.
Các vấn đề liên quan đến nội dung hoặc quyền sở hữu trí tuệ của bài viết, vui lòng gửi email đến info@khanhanlaw.net.
Khánh An là một công ty tư vấn tại Việt Nam có kinh nghiệm và năng lực cung cấp các dịch vụ tư vấn liên quan đến Doanh nghiệp và Đầu tư. Vui lòng tham khảo về dịch vụ của chúng tôi qua website: khanhanlaw.com hoặc liên hệ trực tiếp qua số Hotline: 097.652.9499.
 Trước năm 2022, trang thiết bị y tế nhóm C,D không bắt buộc phải đăng ký lưu hành mà có thể xin giấy phép nhập khẩu hoặc công khai phân loại đối với trang thiết bị y tế không thuộc danh mục phải phê duyệt cấp phép nhập khẩu. Từ 01/01/2022 nghị định 98/2021/NĐ-CP có hiệu lực, đăng ký lưu hành trang thiết bị y tế nhóm C,D phải đăng ký lưu hành. Tuy tại điều khoản chuyển tiếp một số trang thiết bị y tế được phép tiếp tục nhập khẩu đến 31/12/2022, nhưng do tính chất đặc thù của trang thiết bị y tế, một số cơ quan hải quan vẫn yêu cầu buộc phải có số lưu hành trang thiết bị y tế để thông quan hàng hóa. Cùng Khánh An tìm hiểu dịch vụ đăng ký lưu hành trang thiết bị y tế nhóm C,D trong bài viết sau:
Trước năm 2022, trang thiết bị y tế nhóm C,D không bắt buộc phải đăng ký lưu hành mà có thể xin giấy phép nhập khẩu hoặc công khai phân loại đối với trang thiết bị y tế không thuộc danh mục phải phê duyệt cấp phép nhập khẩu. Từ 01/01/2022 nghị định 98/2021/NĐ-CP có hiệu lực, đăng ký lưu hành trang thiết bị y tế nhóm C,D phải đăng ký lưu hành. Tuy tại điều khoản chuyển tiếp một số trang thiết bị y tế được phép tiếp tục nhập khẩu đến 31/12/2022, nhưng do tính chất đặc thù của trang thiết bị y tế, một số cơ quan hải quan vẫn yêu cầu buộc phải có số lưu hành trang thiết bị y tế để thông quan hàng hóa. Cùng Khánh An tìm hiểu dịch vụ đăng ký lưu hành trang thiết bị y tế nhóm C,D trong bài viết sau:
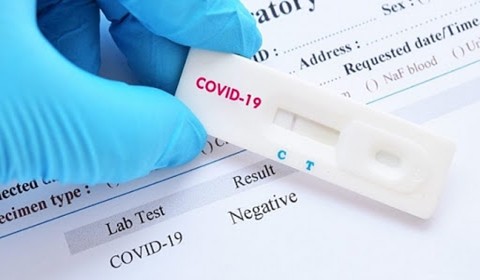 Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus và xét nghiệm tìm kháng thể do cơ thể sinh ra để chống lại virut. Test nhanh covid 19 phát hiện kháng nguyên covid 19 hiện nay đang được ứng dụng rộng rãi để sàng lọc diện rộng nhằm phát hiện covid 19.
Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus và xét nghiệm tìm kháng thể do cơ thể sinh ra để chống lại virut. Test nhanh covid 19 phát hiện kháng nguyên covid 19 hiện nay đang được ứng dụng rộng rãi để sàng lọc diện rộng nhằm phát hiện covid 19.
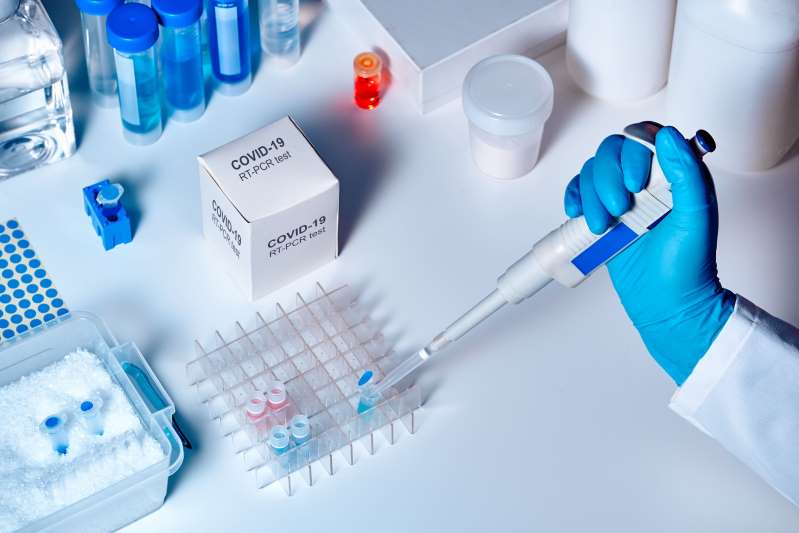 Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus. Test phát hiện kháng nguyên virus SarS-CoV-2 là gì? Kit xét nghiệm đa chỉ tiêu SARS-CoV-2 RT-PCR là hóa chất chuẩn đoán dùng trong xét nghiệm định tính RNA từ vi-rút SARS-CoV-2 bằng phương pháp Real-Time RT-PCR từ các mẫu bệnh phẩm đường hô hấp trên như mẫu phết dịch mũi họng và mẫu phết dịch hầu họng.
Để xét nghiệm SARS-CoV-2, có 2 loại xét nghiệm thường dùng nhất là xét nghiệm tìm kháng nguyên virus. Test phát hiện kháng nguyên virus SarS-CoV-2 là gì? Kit xét nghiệm đa chỉ tiêu SARS-CoV-2 RT-PCR là hóa chất chuẩn đoán dùng trong xét nghiệm định tính RNA từ vi-rút SARS-CoV-2 bằng phương pháp Real-Time RT-PCR từ các mẫu bệnh phẩm đường hô hấp trên như mẫu phết dịch mũi họng và mẫu phết dịch hầu họng.